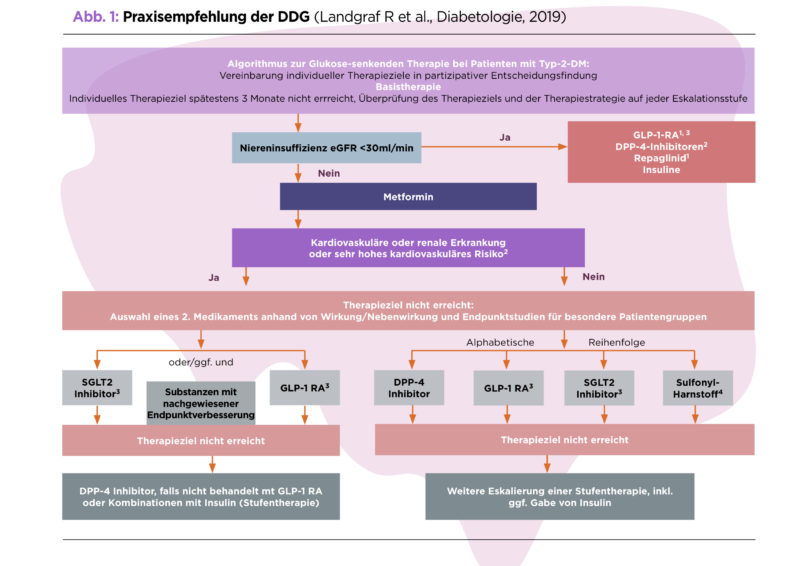
Derzeit sind den NVL-Autoren zufolge die Daten bei den SGLT2-Hemmern für Empagliflozin und bei den GLP-1-RA für Liraglutid am “belastbarsten” [2]. Sie werden aber nicht namentlich im Algorithmus empfohlen, weil sich aktuell die Studienlage zu anderen Wirkstoffen schnell ändere. Die Effekte auf verschiedene Endpunkte – wie Gesamtmortalität, kardiovaskuläre oder renale Ereignisse, HbA1c, Gewicht oder Hypoglykämien – stellt die NVL übersichtlich in Evidenztabellen zusammen. Keine Daten gebe es bislang für die Wirksamkeit einer Kombitherapie bei Diabetikern ohne Herzinsuffizienz und einem HbA1c ≤ 7 Prozent.
“Dank der modernen Antidiabetika ist es uns heute möglich, nicht nur bei manifester kardiovaskulärer oder renaler Erkrankung tätig zu werden, sondern bereits wenn bei einem Diabetes-Patienten entsprechende Risikofaktoren vorliegen”, fasste Diabetologin Prof. Petra-Maria Schumm-Draeger bereits bei einer Fortbildung in München im Februar die Studienlage zusammen [4]. Bei der Verordnung sollten Ärzte jedoch auch die Nutzenbewertung durch den Gemeinsamen Bundesausschuss im Blick haben.
Bei der regelmäßigen Kontrolle soll auch die De-Eskalation thematisiert sowie Nutzen und Schaden der Optionen in absoluten Risiken veranschaulicht werden, heißt es in der NVL. Hierzu soll die NVL künftig Patienteninformationen bereitstellen. Die Effekte seien für SGLT2-Hemmer sowie GLP-1-RA bei vorbestehender kardiovaskulärer Erkrankung konsistent, so die NVL-Autoren. Bei mehreren kardiovaskulären Risikofaktoren fielen die Vorteile hingegen geringer aus. [2]
SGTL2-Hemmer im Fokus
SGLT2-Inhibitoren bewirken über die Hemmung des Natrium-Glukose-Kotransporters 2 (SGLT2) in der Niere eine verringerte renale Glukosereabsorption und somit eine Glukosurie in Abhängigkeit vom Blutzucker und der Nierenfunktion. Dadurch verbessert sich die Blutzuckerkontrolle und es kommt zu einer Gewichtsreduktion, da mehr Kalorien ausgeschieden werden. Die NVL listet Empagliflozin, Canagliflozin, Dapagliflozin und Ertugliflozin auf. [2]
In der EMPA-REG OUTOME-Studie [5] senkte z.B. Empagliflozin im Vergleich zu Placebo die Gesamtmortalität (5,7 versus 8,3 Prozent) sowie kardiovaskuläre Todesfälle (3,7 versus 5,9 Prozent). Ein ähnlicher Effekt zeigte sich bei Diabetikern mit Herzinsuffizienz für Dapagliflozin: Hier lag die Gesamtsterblichkeit bei 13,3 Prozent gegenüber 16,7 Prozent unter Placebo [6].
Die NVL weist darauf hin, dass SGLT2-Hemmer bei gleichzeitiger Anwendung mit Sulfonylharnstoff oder Insulin häufiger zu Hypoglykämien führen können. Ebenso kamen Genitalinfektionen öfter vor. Insbesondere bei älteren Patienten oder bei der parallelen Einnahme von Diuretika sollten Patienten genügend trinken. Um Amputationen vorzubeugen, soll allen Patienten zu routinemäßiger Fußpflege geraten werden. [2]
GLP-1-RA im Überblick
Alternativ oder als Kombinationspartner eines SGLT2-Inhibitors lassen sich GLP-1-RA wie Liraglutid, Exenatid, Albiglutid, Dulaglutid oder Semaglutid einsetzen. Sie regen die Insulinausschüttung an und hemmen die Glukagonfreisetzung. Ebenso verzögern sie die Magenentleerung und mindern den Appetit, wodurch Patienten in der Regel abnehmen. In Studien verbesserten sie renale Endpunkte, jedoch lässt sich laut NVL anhand der Nierenfunktion noch nicht herleiten, welche Patienten am ehesten profitieren. [2]
Unter Liraglutid kam es in der LEADER-Studie zum Beispiel gegenüber Placebo zu weniger kardiovaskulären Todesfällen (4,7 versus 6 Prozent). Hinweise für einen positiven Effekt zeigten sich bei Gesamtmortalität (8,2 versus 9,6 Prozent) und einer geringeren Zahl renaler Ereignisse (kombinierter Endpunkt 5,7 versus 7,2 Prozent). Vorteile ergaben sich vor allem bei Patienten mit manifester kardiovaskulärer Erkrankung und Patienten mit einer eGFR < 60 ml/min/1,73m2. [7]
Als einziger oraler GLP-1-RA ist in der EU inzwischen Semaglutid zugelassen [8], dies war bei der Erstellung der NVL noch nicht der Fall. Die Kombination mit einem Hilfsstoff (SNAC) ermöglicht die Resorption des Wirkstoffs über die Magenschleimhaut. Im Vergleich zu Liraglutid zeigte sich orales Semaglutid bei der Senkung des HbA1c (-1,2 versus -1,1 Prozent nach 26 Wochen) als nicht unterlegen, gegenüber Placebo (-0,2 Prozent) als überlegen. Zudem verloren die Teilnehmer unter Semaglutid am meisten Gewicht (-4,4 kg), bei Liraglutid waren es 3,1 kg weniger und bei Plaecbo nur -0,5 kg. [9]
Bei GLP-1-RA kommen laut NVL vor allem gastrointestinale Nebenwirkungen vor. Patienten sollten daher über das Erscheinungsbild einer akuten Pankreatitis aufgeklärt werden. Meist nehmen Patienten unter der Therapie ab: Dies wird in der Regel als positiv gesehen, Vorsicht sei deswegen aber bei älteren, gebrechlichen Patienten geboten. Darüber hinaus kann die Anwendung bei Niereninsuffizienz eingeschränkt sein, so die NVL. Zudem könnte die Injektion nicht von jedem Patienten gewünscht sein, auch wenn Reaktionen an der Injektionsstelle eher selten auftreten. [2]
Diabetes-Typ-2 und Herzinsuffizienz
Patienten mit Typ-2-Diabetes haben ein zwei- bis vierfach erhöhtes Risiko für eine Herzinsuffizienz, die häufig schon in jüngeren Jahren auftritt. Dies verschlechtert ihre Prognose bei kardiovaskulärer und Gesamtmortalität. [10] Studien zufolge können neue Therapeutika aber die Prognose günstig beeinflussen, die NVL Diabetes verweist hierzu auf die NVL Herzinsuffizienz [2].
Vor allem die DAPA-HF-Studie mit Dapagliflozin und jüngst die EMPEROR-Reduced-Studie mit Empagliflozin haben Vorteile gezeigt. So senkte Dapagliflozin nur bei Diabetikern mit Herzinsuffizienz die Gesamtmortalität verglichen mit Placebo (13,3 versus 16,7 Prozent). Auch der kombinierte Endpunkt aus kardiovaskulären Todesfällen und Hospitalisierung wegen Herzinsuffizienz war seltener (16,3 versus 21,2 Prozent) [11]. Die NVL-Gruppe hält einen Klasseneffekt der SGLT2-Hemmer für “plausibel”.
“Wichtig ist, dass die Therapie der Herzinsuffizienz leitlinienkonform, gemäß des Stufenschemas erfolgt und dass von diesem Schema nicht aufgrund eines zusätzlich vorliegenden Diabetes-Typ-2 abgewichen wird”, betont Priv.-Doz. Dr. Wibke Hengstenberg [10]. Bei einer Herzinsuffizienz mit reduzierter Ejektionsfraktion (HFrEF) umfasst die erste Therapiestufe einen ACE-Hemmer sowie einen Beta-Blocker, welche ggf. mit weiteren Präparaten ergänzt werden [12]. Rund die Hälfte der Patienten mit HFrEF weise einen Eisenmangel auf. Dieser solle unbedingt behandelt werden, da er – unabhängig vom Vorliegen einer Anämie – negative Folgen für den Organismus hat [10].
Im Gegensatz zu SGLT2-Inhibitoren oder GLP-1-RA sei Saxagliptin nicht geeignet für Diabetes-Patienten mit Herzinsuffizienz, da es unter diesem DPP-4-Inhibitor zu signifikant mehr Krankenhauseinweisungen komme. Andere Vertreter der Substanzklasse wie Sitagliptin oder Linagliptin wiesen diesen Effekt jedoch nicht auf. “Bei Insulin und Sulfonylharnstoffen nehmen die Sicherheitsbedenken zu und Glitazone sind im Rahmen der antidiabetischen Therapie bei Herzinsuffizienz kontraindiziert”, resümierte Hengstenberg. [10]
Quellen:
- Buse JB et al. Diabetologia. 2020 Feb; 63(2): 221-228
- Nationale Versorgungsleitlinie Diabetes, Konsultationsfassung, veröffentlicht 27.8.2020
- Landgraf R et al. Diabetologie 2019; 14 (Suppl 2): 103–324
- Patientenforum: Diabetes, Herz, Gefäße: “Fit” mit modernen Medikamenten und der richtigen Bewegung. Anlässlich “Innere Medizin fachübergreifend – Diabetologie grenzenlos”, München, 7.2.20
- Zinman B et al. N Engl J Med 2015; 373: 2117-2128
- Petrie MC, Verma S, Docherty KF, et al. Effect of Dapagliflozin on Worsening Heart Failure and Cardiovascular Death in Patients With Heart Failure With and Without Diabetes. JAMA 2020; 323(14):1353-1368. DOI: 10.1001/jama.2020.1906
- Marso SP, Daniels GH, Brown-Frandsen K, et al. Liraglutide and Cardiovascular Outcomes in Type 2 Diabetes. N Engl J Med 2016; 375(4):311–22. DOI: 10.1056/NEJMoa1603827. http://www.ncbi.nlm.nih.gov/pubmed/27295427
- Pressemitteilung Novo Nordisk Pharma, 21.4.20
- Pratley R et al. Lancet. 2019 Jul 6; 394(10192): 39-50
- Chronische Herzinsuffizienz: Unterschätzte Gefahr bei Diabetes mellitus. Anlässlich “Innere Medizin fachübergreifend – Diabetologie grenzenlos”, München, 7.2.20
- Nationale Versorgungsleitlinie Chronische Herzinsuffizienz, 3. Aufl. 2019 Version 2, gültig bis 22.10.24
- Ponikowski P, et al. Eur Heart J. 2016 Jul 14; 37(27): 2129-2200