 © DAP
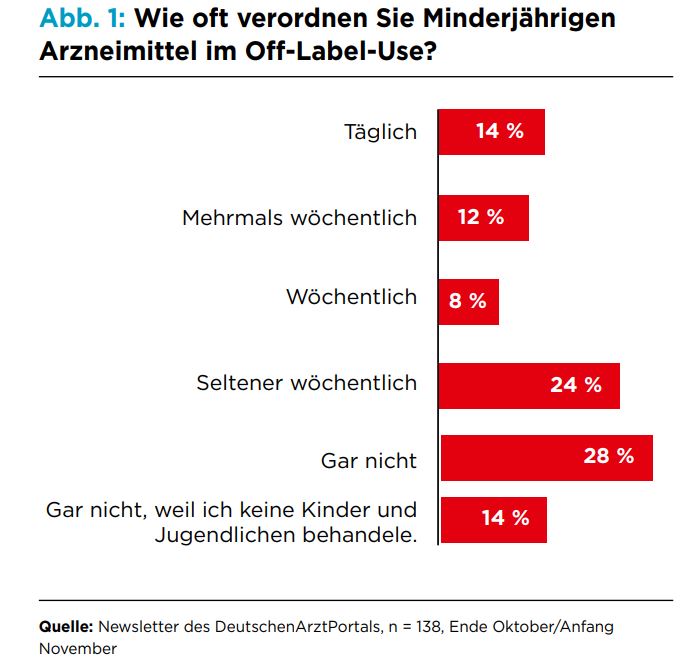
© DAPUmfrageergebnisse: Wie oft verordnen Sie Minderjährigen Arzneimittel im Off-Label-Use?
Abhilfe durch die EU-Kinderverordnung
In der Regel werden Arzneimittel zunächst mit Erwachsenen und erst im Anschluss mit Kindern und Jugendlichen untersucht, wodurch letztere einen besonderen Schutz genießen. In der Vergangenheit fanden klinische Studien mit Kindern und Jugendlichen jedoch oft gar nicht statt – bis in die 1980er Jahre gab es ethische Vorbehalte.
Die daraus resultierende ungleich schlechtere Arzneimittelversorgungslage für Kinder und Jugendliche erkannte auch die EU und beschloss die sogenannte Kinderverordnung, die Anfang 2007 in Kraft trat. [1, 7, 8]
Kern der EU-Verordnung ist ein verpflichtendes pädiatrisches Prüfkonzept (PIP, Paediatric Investigation Plan), das bei Einreichung der Zulassungsunterlagen für ein neues Arzneimittel vorgelegt werden muss und ein geplantes Entwicklungsprogramm für die Anwendung an Kindern enthält. Von dieser Verpflichtung ausgenommen sind u. a. Generika und Biosimilars, da in diesen Fällen eine gleichwertige Wirksamkeit und Sicherheit wie beim Originalpräparat für alle Altersklassen angenommen werden.
Der wissenschaftliche Pädiatrieausschuss (PDCO, Paediatric Committee) der Europäischen Arzneimittel-Agentur (EMA) bildet dabei die zentrale Kontrollstelle. Fehlt etwa ein vom Ausschuss genehmigtes Prüfkonzept für Minderjährige, wird der Zulassungsantrag als unvollständig zurückgewiesen. Der Pädiatrieausschuss kann beispielsweise verlangen, dass
- Arzneimittelstudien auch für bestimmte Altersklassen (Kinder und/oder Jugendliche) erfolgen,
- eine kindgerechte Darreichungsform entwickelt wird,
- Studien für Kinder und/oder Jugendliche parallel oder im Anschluss zu Erwachsenenstudien stattfinden. [1, 9]
Die EU zog 2017 zehn Jahre nach Einführung der Kinderverordnung ein positives Zwischenfazit: Von 2007 bis 2016 stieg der Anteil klinischer Studien mit Kinderbeteiligung in der EU von 8,25 auf 12,4 Prozent, über 250 neue Arzneimittel wurden für Kinder und Jugendliche zugelassen sowie mehr als 1.000 PIP angenommen, wovon 131 im genannten Zeitraum abgeschlossen wurden. [8]
Neuere Zahlen bestätigen die positive Entwicklung: Zwischen 2021 und 2023 wurden jährlich 46 bis 52 neue Medikamente und Applikationshilfen für Kinder und Jugendliche neu zugelassen, die zuvor höchstens für höhere Altersklassen bei Minderjährigen oder Erwachsene verfügbar waren. [2] Insbesondere für seltene und onkologische Erkrankungen besteht aber noch viel Potenzial bei der Entwicklung von Kinderarzneimitteln. [8]
Lieferengpässe: Was hilft?
Während sich die Situation bei den zugelassenen Arzneimitteln in den letzten zwei Jahrzehnten für Kinder und Jugendliche insgesamt positiv entwickelt hat, wurden sowohl Ärztinnen und Ärzte als auch das Apothekenpersonal mit einer neuen Hürde konfrontiert: Lieferengpässe (siehe Artikel “Besorgter Blick auf den Winter” HA 16/24).
Zu oft fehlten in den ausklingenden Covid-19-Pandemiejahren dringend benötigte Fiebersäfte oder Antibiotika für die Kleinsten. Die Gründe hierfür sind vielfältig, u. a. eine Konzentrierung der Produktion auf wenige – meist asiatische – Länder sowie fehlende finanzielle Anreize für Pharmahersteller und starke Infektionswellen. Der Gesetzgeber reagierte 2023 mit dem Arzneimittel-Lieferengpassbekämpfungs- und Versorgungsverbesserungsgesetz (ALBVVG). [10]
Mit dem ALBVVG wurden u. a. Festbeträge und Rabattverträge für Kinderarzneimittel abgeschafft und Hersteller durften den Preis einmalig um 50 Prozent anheben. In Apotheken wurden die Austauschregeln bei Nichtverfügbarkeit eines Arzneimittels erleichtert – diese gelten auch für nicht verfügbare Arzneimittel für Erwachsene.
In diesen Fällen dürfen Apotheken ohne ärztliche Rücksprache, etwa bei der abgegebenen Packungsgröße, Packungsanzahl und Wirkstärke (verordnete Wirkstoff-Gesamtmenge darf nicht überschritten werden) von der Verordnung abweichen.
Darüber hinaus dürfen Apotheken bei Nichtverfügbarkeit eines Kinderarzneimittels der Dringlichkeitsliste des Bundesinstituts für Arzneimittel und Medizinprodukte (BfArM) dieses gegen ein wirkstoffgleiches in der Apotheke hergestelltes Arzneimittel, auch in einer anderen Darreichungsform, oder gegen ein wirkstoffgleiches Fertigarzneimittel in einer anderen Darreichungsform ohne ärztliche Rücksprache austauschen. [10, 11]
Inwieweit die Maßnahmen Wirkung gezeigt haben, bleibt umstritten – Lieferengpässe stellen weiter eine große Herausforderung für alle Beteiligten des Gesundheitssystems dar. Ende Oktober 2024 wurden für 490 Arzneimittel Lieferengpässe durch das BfArM gemeldet. [12] Davon betroffen sind u. a. Antibiotika und atomoxetinhaltige Arzneimittel. Bei paracetamol- und ibuprofenhaltigen Fiebersäften sind laut BfArM keine Lieferengpässe bekannt (Stand: September 2024).
Dennoch empfiehlt das BfArM mit Blick auf die laufende Infektionssaison, die Verordnung einer festen oralen Darreichungsform unter Berücksichtigung des Alters der Patientin oder des Patienten und der Verfügbarkeit der Darreichungsform zu prüfen. [12, 13] Die Deutsche Gesellschaft für Pädiatrische Infektiologie e.V. (DGPI) gibt darüber hinaus Empfehlungen zu Alternativen bei der antibiotischen Therapie im Falle von Versorgungsengpässen. [14]
Fazit
- Kinder und Jugendliche hatten bei Arzneimitteln lange das Nachsehen. Auch heute noch müssen Ärztinnen und Ärzte bei Verordnungen für Kinder und Jugendliche teilweise auf Arzneimittel im Off-Label-Use zurückgreifen.
- Durch die EU-Kinderverordnung sind zwar mehr Kinderarzneimittel klinisch erprobt und zugelassen, jedoch machen Lieferengpässe auch und vor allem vor Kinderarzneimitteln nicht Halt.
- Gerade bei Off-Label-Use sollten Ärztinnen und Ärzte auf eine gute Dokumentation achten, um Regresse zu vermeiden.
Quellen:
- https://www.bfarm.de/DE/Arzneimittel/Zulassung/Arzneimittel-fuer-Kinder/_node.html
- https://www.vfa.de/de/arzneimittel-forschung/datenbanken-zu-arzneimitteln/amzulassungen-kinder.html/_p6#listmedikamentekinder-90722
- https://www.kinderformularium.de/sign_in/startseite
- Umfrage DeutschesArztPortal vom 22.10. bis 03.11.2024 “Wie oft verordnen Sie Kindern und Jugendlichen Arzneimittel im Off-Label-Use?”
- Gemeinsamer Bundesausschuss, Off-Label-Use – Verordnungsfähigkeit von Arzneimitteln in nicht zugelassenen Anwendungsgebieten
- VIN VerordnungsInfo KV Nordrhein “Off-Label-Use-Verordnung von Arzneimitteln außerhalb der Zulassung” vom 7. Juli 2022
- Verordnung (EG) Nr. 1901/2006 des Europäischen Parlaments und des Rates vom 12. Dezember 2006
- State of Paediatric Medicines in the EU, 10 years of the EU Paediatric Regulation, 2017
- https://www.vfa.de/de/arzneimittel-forschung/arzneimittel-fuer-kinder/eu-kinderam-vo.html
- https://www.bundesgesundheitsministerium.de/ministerium/gesetze-und-verordnungen/guv-20-lp/albvvg
- https://www.bfarm.de/DE/Arzneimittel/Arzneimittelinformationen/Lieferengpaesse/ALBVVG/_node.html
- Lieferengpass-Datenbank des Bundesinstituts für Arzneimittel und Medizinprodukte
- https://www.bfarm.de/DE/Arzneimittel/Arzneimittelinformationen/Lieferengpaesse/mitteilung_fiebersaefte_kinder.html?nn=471282
- https://dgpi.de/versorgungsengpaesse-antibiotika-20-12-2022/